最新消息,由清华大学、深圳市第三人民医院和腾盛博药合作研发的新冠药物BRII-196和BRII-198联合用药临床Ⅲ期已揭盲,给药组在治疗28天后实现零死亡,对照组8例死亡,详细结果会在近期对外公布。这也是目前我国进展最快的抗体药物,有望12月底前获得批准附条件上市。与欧美已获批紧急使用的新冠抗体药相比,该药是唯一进行了变异株感染者治疗效果评估并获得数据的。
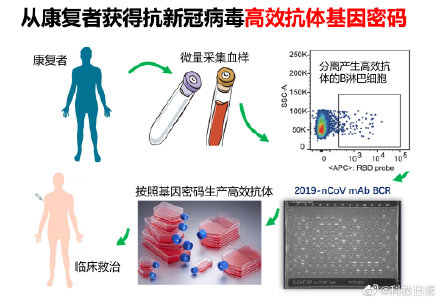
研发团队:不信捷径,从头研发
新冠疫情初期有效药匮乏,一些基于MERS(中东呼吸综合征)、艾滋病病毒进行研发的药物被寄予厚望。
2020年4月的一次学术交流上,项目带头人张林琦曾表示,从科学上讲,抗其他病毒的药对新冠病毒有效的可能性太小了。新冠病毒特效药必须从研究新冠病毒开始,有针对性地开发。
“不信捷径、从头研发”的科学精神和态度让清华团队不仅起步早,也少走弯路。
全球都在寻找最有效的中和抗体药物,清华团队为什么瞄得更准?
“我们不仅寻找感染者免疫系统中活性好的中和抗体,还研究它们的‘家谱’,开展综合分析和判断。”张林琦说,比如,两个“姐妹”关系的抗体有什么样的共同特点,通过微观水平的比较,能够发现抗体结构与抗病毒活性的关系,这些重要线索,为挑选我们精英中的精英抗体发挥了至关重要的指导作用。
此外,针对病毒变异,团队不仅先病毒一步,也先人一步——
先病毒一步,团队在精细结构解析的基础上,利用28种突变假病毒评估了12种中和抗体的中和能力,早于变异发生前获得引发抗体失效的病毒变异规律。
先人一步,团队凭借丰富的抗病毒药物研发经验,在临床试验早期就评估其候选抗体组合BRII-196/BRII-198对变异株的中和活性,有效避免了“上了战场”却被病毒逃逸的情况发生。
相较而言,全球其他研发团队中已有多个中和抗体候选药物在三期临床时被证明对病毒变异株无效。
多部门:滚动立项、启动核查、协同推进
由于我国新冠疫情控制良好,研发走向临床时面临“入组患者不足、临床试验进展缓慢”的困局。为推动我国新冠特效药顺利上市,科研攻关组各部门之间积极沟通、研审联动。科技部积极跟进研发进展,协调解决困难,药监局多次就附条件上市问题与研发团队沟通,并启动药品注册临床试验现场核查等工作……
一方面,科研攻关组积极推动对中和抗体应急项目的滚动支持,通过专家的严格审评和大力推荐,及时高效地完成对BRII-196和BRII-198中和抗体联合疗法的滚动立项支持,支持团队在国内开展由钟南山院士牵头的二期临床试验,加快国内临床试验进度。
另一方面,清华大学、深圳市第三人民医院和腾盛博药开启联合研发。基于国内一期临床试验数据的支持,2020年12月,BRII-196和BRII-198抗体组合药物顺利进入由美国国立卫生研究院发起的新冠药物临床研究平台,开启了高标准、严要求的国际多中心随机、双盲、对照二期和三期临床试验。在4大洲、6个国家、111个临床试验机构进行的837例新冠肺炎患者三期临床试验结果显示,抗体组合药物能够降低78%的住院和死亡率,且给药组在治疗28天后实现零死亡,对照组8例死亡。
据介绍,目前BRII-196和BRII-198联合用药有望实现在我国附条件批准上市与美国紧急使用的同步。
高分答卷:面对“拖延”患者,疗效仍显著
项目团队提供的资料显示,临床试验设计质量高、难度大,验证了联合药物对不同地区(多中心)、不同种族(多种族)人群和多种新冠病毒变异株(多变异株)的治疗均有效。对于那些确诊时间较长(10天以内)、病情被“拖延”、病情相对较重的患者治疗效果仍非常明显。此外,经过基因改造,该药半衰期是普通抗体的2—3倍,在体内有效作用时间可长达数月。据介绍,该药对未感染的高危人群也可产生预防保护作用,相关研究和分析正在进行之中。
在国际上,已有同类型抗体药物获批紧急使用,美国再生元公司的中和抗体使住院及死亡率下降70%,葛兰素史克/Vir生物技术公司的中和抗体使住院及死亡率下降79%,但这两款中和抗体临床试验均不包含变异株数据,且入组受试者为确诊发病5—7日内的患者。相较而言,BRII-196和BRII-198的入组受试者为发病10日内,病情在体内发展了更长时间,治疗难度更大,依然得到78%的显著保护数据。
文章内容来源于网络,不代表本站立场,若侵犯到您的权益,可联系多特删除。(联系邮箱:9145908@qq.com)
 相关阅读
相关阅读










 近期热点
近期热点
 最新资讯
最新资讯